FDA发文警告!继亚硝胺之后,又一焦点致癌物出现了?
来源:药智网/骎丹翼

自从2018年发生的沙坦类药物的亚硝胺杂质事件之后,FDA一直在加紧制药公司和CDMO对于API与制剂中亚硝胺杂质的监控管理。
而如今,苯污染成为了FDA关注的下一个致癌杂质。
据悉,相关制药公司已经开始陆续接受到FDA的信件,要求对可能被苯污染的药物进行风险评估。
目前,FDA正在评估某些药物中苯污染的根本原因,并提醒药品制造商注意药物成分和其他造成苯污染的潜在风险。
明确人类致癌物
苯是一种已知的人类致癌物,会导致白血病和其他血液疾病。
由于苯污染,某些洗手液和气雾剂药品已被召回。这种污染可能与制剂中的非活性成分,诸如卡波姆(Carbo-mer,增稠剂)、异丁烷(喷雾推进剂)或其他由碳氢化合物制成的药物成分有关。
FDA提醒药品制造商,他们需要建立科学且适当的规范和测试程序,以确保药物成分(活性和非活性成分)和成品药符合适当的质量规范(21 CFR 211.84、21 CFR 211.160)。这包括在放行前对原材料和成品批次(21 CFR 211.165)进行测试,以确保它们符合适当的特性、效果、质量和纯度规范。
使用风险评估等工具是应对这种局面的有效手段之一,药物制造商以此来确定他们是否具有适当的测试方法和控制措施,以确保药物不受污染。FDA已与制造商讨论进行风险评估,以评估其药品和成分(包括活性成分和非活性成分)中可能存在的苯。
FDA特别强调,需要尤其关注碳氢化合物,以及使用苯或其他碳氢化合物为原料制造出来的药物成分(包括赋形剂)。
基于明确的人类致癌物身份,FDA责令制造商不应在制造药物时使用苯。ICH Q3C杂质规定,1类溶剂(例如苯)由于具有不可接受的毒性,因此不应用于原料药、赋形剂或药品的生产。该指南指出,如果苯的使用不可避免地用于生产具有显著治疗效果的药物产品,则其水平应限制在2 ppm以下。
苯含量超标情况层出不穷
然而在现实中,苯含量超标的情况层出不穷。
除了FDA在今年的几封警告信中指出的消毒剂苯超标之外,很多化妆用品中的苯含量也令人担忧。
美国独立QA实验室Valisure分析了来自69个不同品牌的294个独特的防晒霜批次。他们发现27%的样品具有可检测水平的苯。有些含有高达FDA推荐允许量的3倍。在喷雾剂、乳液和凝胶中也发现了苯污染。一些产品的化学和矿物基配方被发现含有苯。
来自四家公司(Sun Bum、Neutrogena、Fruit of the Earth和CVS)的14种产品含有2.8–6.3ppm的苯。这些水平(大于2ppm)超过了FDA的安全限制。
来自8个不同品牌的26种产品的苯含量在0.11–1.99 ppm之间,低于2 ppm的水平符合FDA的建议。来自17个品牌的38种产品的苯含量低于0.1ppm。
值得注意的是,防晒霜并不遵循FDA的苯含量低于2 ppm的质量标准,但在这些产品中检测出苯,仍然不是什么好事情。
药品中的苯限量?
在FDA评估某些药物中苯污染的根本原因时,他们正在采取逐步的方法来解决上市药品中苯污染的可能性,方法是首先根据ICH指南中描述的注意事项,确认那些苯含量高于2 ppm的产品,哪些应该召回,哪些不应放行。
同时,FDA还将审查来自药品制造商的确定存在苯的现场警报报告。该信息将有助于进一步更新FDA酌情限制药品中苯含量的方法。
FDA注意到,某些美国药典(USP-NF)的卡波姆(Carbo-mer)专论允许苯含量为100 ppm或更高。为了消除混淆,并且由于与这些不可接受的苯水平相关的安全问题,FDA已要求USP从他们的纲要中删除(或“省略”)这些专论。
为了确保产品符合适当的质量规范(21 CFR 211.84、21 CFR 211.160),并符合ICH Q3C指南中的建议,那些确定药物苯污染风险或确认苯存在于药品中的申请人和制造商,还应采取措施使用不含苯的成分,或者将不可接受的苯杂质水平的风险降至最低。FDA打算为制造商发布关于推荐测试方法的指南,以及制造商需要修改其合法上市药品的配方或制造工艺的适当步骤。
药品制造商应该怎么做?
药品制造商必须确保其药品的安全性和质量。与ICH Q3指南的建议一致,制造商不应在药物制造中使用苯。碳氢化合物或用苯或其他碳氢化合物制造的成分可能受到苯污染。
FDA还注意到一些成分,例如抗真菌防腐剂苯甲酸钠(benzoate),在某些条件下可能会形成苯(图2)。FDA提醒制造商,在整个药物生命周期中原材料的变化,包括原材料供应商的变化,需要对苯污染的潜在风险进行额外的审查。
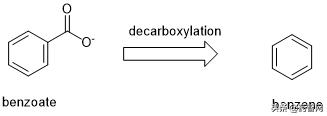
苯甲酸盐脱羧降解为苯的化学过程
图片来源:参考资料
FDA提醒NDA和ANDA产品的制造商,如果测试显示他们的药品中苯含量超过2 ppm(21 CFR 314.81(b)(1)(ii)),他们有义务提交现场警报报告(FAR)。
参考来源:
Bass,D.The carcinogen benzene is found in several sunscreen products.02,06,2021.https://sheaaestheticclinic.com/blog/the-carcinogen-benzene-is-found-in-several-sunscreen-products
FDA alerts drug manufacturers to the risk of benzene contamination in certain drugs
https://www.fda.gov/drugs/pharmaceutical-quality-resources/fda-alerts-drug-manufacturers-risk-benzene-contamination-certain-drugs
版权声明:CosMeDna所有作品(图文、音视频)均由用户自行上传分享,仅供网友学习交流。若您的权利被侵害,请联系删除!
本文链接://www.cosmedna.com/article/891474471.html





































